
 热点栏目
自选股
数据中心
行情中心
资金流向
模拟交易
客户端
热点栏目
自选股
数据中心
行情中心
资金流向
模拟交易
客户端
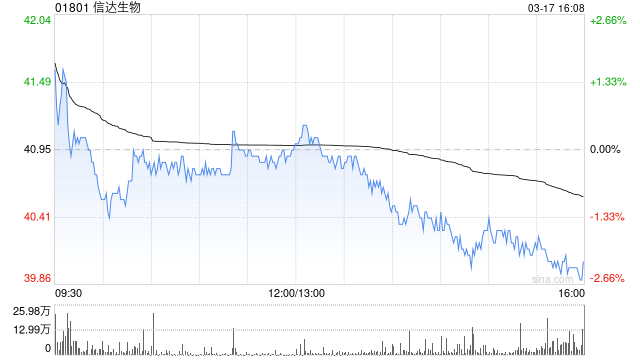
中金发布研究报告称,维持信达生物(01801)“跑赢行业”评级,24/25收入及盈利预测不变,基于DCF模型,由于公司管线临床数据持续兑现,该行认为管线价值潜力提升,上调目标价4.2%至50港元。公司近期于2024年ASCO大会及ESMO
7月1日,新能源车企相继交出“成绩单”。其中,比亚迪、蔚来、极氪、零跑均刷新单月销量、交付纪录。
Plenary披露三项肿瘤管线产品积极数据,临床数据积极读出叠加公司高效临床推进策略,该行认为公司肿瘤管线有望不断充实,建议关注IBI363等肿瘤产品未来进一步数据披露。
中金主要观点如下:
IBI363(PD-1/IL2双融合蛋白)早期小样本临床数据积极,关注产品用于IO经治实体瘤患者未来治疗潜力。
IBI363本次公布Ia/Ib期研究,截至24年4月16日,共入组347例受试者(包括100例NSCLC,89例黑色素瘤和102例CRC患者及其他实体瘤患者),患者接受0.2μg/kg
QW-3mg/kg
Q3W不同剂量治疗,剂量递增阶段IBI363在NSCLC、黑色素瘤及结直肠癌均呈现出积极的初步治疗结果响应。其中9例高剂量组肺癌患者数据值得关注,其中8例既往接受过PD-(L)1治疗,1例接受过TCE治疗,患者接受3mg/kg
Q3W给药,6例肺鳞癌患者ORR
100%。该行认为高剂量组数据在sqNSCLC早期值得关注,公司预计后续将进一步探索IBI363单药在肺癌以及黑色素瘤后线治疗的潜力,并将探索IBI363联合ADC等产品的进一步治疗潜力,建议关注IBI363后续临床开展动向及数据读出节奏。
CLDN18.2双抗及ADC产品IBI389&IBI343临床高效推进,PDAC展现积极治疗潜力。
IBI343目前正在开展单药治疗CLDN18.2阳性,HER2阴性的mGC/GEJ的全球III期临床。本次ASCO大会,公司公布IBI343治疗至少接受过一线治疗的胰腺癌患者的I期初步数据,结果显示在接受6mg/kg药物治疗的CLDN18.2中高表达(IHC1/2/3+≥60%)的10例患者中,ORR为40%。目前FDA已授予IBI343治疗CLDN18.2表达阳性晚期胰腺导管腺癌的快速通道资格。该行认为胰腺癌晚期患者治疗依旧以系统性化疗为主,IBI343早期数据具备潜力,建议积极关注进一步数据读出。此外,CD3/CLDN18.2双抗IBI389同样展现出在胰腺癌和胃癌的早期积极数据响应,该行预计IBI389&IBI343未来将在胰腺癌和胃癌形成组合拳布局。
关注报表减亏预期及产品销售放量节奏。
23年信达生物三费控制良好,研发费用同比下降
22%,管理费用同比下降10%,销售及市场推广费用相较22年降低6.9个百分点,产品端收入稳中有升,该行预计25年公司将有多款慢病产品开启收入兑现。建议积极关注公司报表端向好趋势。
风险
管线进度不及预期;商业化不及预期;产品降价超预期。
MACD金叉信号形成,这些股涨势不错!
 海量资讯、精准解读,尽在新浪财经APP
海量资讯、精准解读,尽在新浪财经APP
责任编辑:史丽君 证券公司股票